问题
填空题
(6分)铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-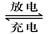 2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
(1)放电时:正极的电极反应式是 ;当外电路通过1mol电子时,电解液中消耗H2SO4 mol。
(2)充电时,Pb 和电源的 极相连,此时发生的电极反应式为 。
答案
(1)PbO2+2e-+4H++SO42-=PbSO4+2H2O 1
(2)负 PbSO4+2e-=Pb+SO42-
(1)放电相当于原电池,在原电池中正极得到电子,根据反应式可知,二氧化铅得到电子,所以正极反应式为PbO2+2e-+4H++SO42-=PbSO4+2H2O。根据总反应式可知,每消耗2mol硫酸,反应中就转移2mol电子,所以如果通过1mol电子,则消耗1mol硫酸。
(2)充电相当于放电的逆反应,放电是铅是负极失去电子,所以充电时铅和电源的负极相连,作阴极,得到电子,所以反应式为PbSO4+2e-=Pb+SO42-。
