问题
填空题
(6分)现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。为确定其组成,进行了如下图所示的实验。
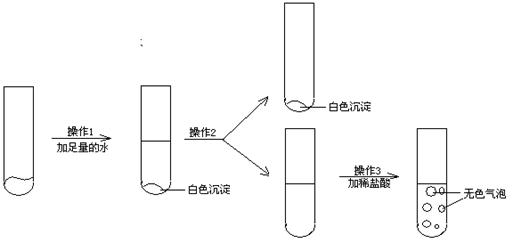
请回答:
(1)操作2的名称是 。
(2)根据实验可以确定白色沉淀是 ;操作3完成后的溶液中一定含有的溶质是 ;
(3)原固体粉末中一定含有 ,它的可能组成有哪几组
(组之间用“;”隔开)。
(4)小明各取CaCO3、CaO、Na2CO3粉末倒入试管,重复以上实验,却与以上现象不完全相同,他的操作没有失误之处,请指出现象不同之处及原因 。
答案
(1)过滤(2)CaCO3;NaCl(3)Na2CO3, Na2CO3、CaCO3;Na2CO3、CaO;Na2CO3、CaCO3、CaO (4)最后一步没气泡,CaO取多了
根据图示(1)除去不溶性固体的方法是过滤;(2)此题中不溶于水的白色一定是碳酸钙,操作三中含有的溶质是碳酸钠。(3)由操作2,混合物中不再含有碳酸钙,但经操作3后再加盐酸有出现了气泡,说明混合物中有碳酸根离子,即为碳酸钠。还可能有的组合是:Na2CO3、CaCO3;Na2CO3、CaO;Na2CO3、CaCO3、CaO;(4)最后一步没气泡,CaO取多了
