物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。
请根据所学知识的回答:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为_______________。
(2)B为0.1 mol·L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(用离子方程式表示):
__________________;实验测得NaHCO3溶液的pH > 7,请分析NaHCO3溶液显碱性的原因:________________________。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入________________________,目的
是________________________;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为____________________。
(4)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:AgCl(s)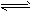 Ag+(aq)+ Cl-(aq) 在25℃时,氯化银的Ksp = 1.8×10-10 25℃时现将足量氯化银分别放入①100mL蒸馏水中②100mL
Ag+(aq)+ Cl-(aq) 在25℃时,氯化银的Ksp = 1.8×10-10 25℃时现将足量氯化银分别放入①100mL蒸馏水中②100mL
0.2 mol·L-1AgNO3溶液中③100mL 0.1 mol·L-1氯化铝溶液中④100mL 0.1 mol·L-1盐酸溶液中。充分搅抖后,相同温度下银离子浓度由大到小的顺序是___________________(填写序号);②中氯离子的浓度
为____________mol·L-1。
(1)c(NH4+) > c(SO42-) > c(H+) >c(OH-)
(2)HCO3- H++CO32-、HCO3+H2O
H++CO32-、HCO3+H2O H2CO3+OH-、H2O
H2CO3+OH-、H2O H++OH-;HCO3-的水解程度大于其电离程度,溶液中c(OH-) > c(H+),故溶液显碱性
H++OH-;HCO3-的水解程度大于其电离程度,溶液中c(OH-) > c(H+),故溶液显碱性
(3)盐酸;抑制Fe3+水解;Fe3++3HCO3-== Fe(OH)3↓+3CO2↑
(4)②①④③;9×10-10
