运用相关原理,回答下列各小题:
Ⅰ.已知NaHSO4在水中的电离方程式为NaHSO4=Na++ H++ SO42- 。
(1)在NaHSO4溶液中c(H+)_________c(OH-)+ c(SO42-)(填“>”、“=”或“<”下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH___________7(2)将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为:_________________;向此反应后的溶液中滴加 0.001 mol·L-1BaCl2溶液,首先析出的沉淀是_____________。[KSP(BaSO4)=1.1×10-10mol2·L-2 ;KSP(BaCO3)=5.1×10-9mol2·L-2]
Ⅱ.已知:在25时 H2O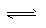 H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH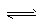 H++CH3COO- Ka=1.8×10-5
H++CH3COO- Ka=1.8×10-5
(3)醋酸钠水解的平衡常数Kh的表达式为___________ 。当升高温度时,Kh将___________(填“增大”“减小”“不变”);
(4)0.5mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a;1mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为__________,a与b的关系为________(填“大于”“小于”“等于”);
(5)0.9mol·L-1醋酸钠溶液中[OH-]= mol·L-1 在某溶液中含Mg2+、Cd2+、Zn2+三种离子的浓度均为0.01mol·L-1。向其中加入固体醋酸钠,使其浓度为0.9mol·L-1,以上三种金属离子中___________能生成沉淀,原因是______________。(KSP[Mg(OH)2]=1.8×10-11、KSP[Zn(OH)2]=1.2×10-17、 KSP[Cd(OH)2]=2.5×10-14、 =2.2)
=2.2)
(1)= ; >
(2)CO32-+H+ === HCO3- ; BaSO4
(3)Kh=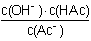 ;增大
;增大
(4)小于;大于
(5)[OH-]=2.2×10-5mol·L-1 Cd2+、Zn2+;
[OH-]=2.2×10-5mol·L-1
[M2+][OH-]2=5×10-12(mol·L-1)
3.5×10-12小于KSP[Mg(OH)2]=1.8×10-11
5×10-12大于KSP[Zn(OH)2]=1.2×10-17
5×10-12大于KSP[Cd(OH)2]=2.5×10-14
