现有部分短周期主族元素的性质与原子(或分子)结构如下表:
| 元素编号 | 元素性质与原子(分子)结构 |
| A | 族序数等于周期数3倍的元素 |
| B | 周期数等于族序数3倍的元素 |
| C | 常温下气体单质为双原子分子.C的气态氢化物能使酚酞溶液变红色 |
| D | 第三周期金属元素,能和B的最高价氧化物对应的水化物反应生成氢气 |
(2)元素B和D相比,金属性较强的是______(填元素符号),可以验证该结论的实验是______.
①比较两种元素的单质的密度
②将这两种元素的单质粉末分别和同浓度的盐酸反应
③将在空气中放置已久的这两种元素的块状单质分别放入热水中
④比较这两种元素的气态氢化物的稳定性
(3)元素B和A能形成化合物B2A2,将10g含有CO2和CO的混合气体,通入装有足量B2A2的干燥管,反应后干燥管的总质量增加5.6g,则原混合气体中的CO2质量分数为______
(4)向某无色透明的溶液中加入D的粉末,反应后只生成氢气.下列各组离子在该溶液中一定可以大量共存的是______
A.K+ Na+ Cl- SO42- B.Na+ Cl- SO42- HCO3-
C.Na+ CO3- NO3- K+ D.Al3+ NH4+ Cl- SO42-.
短周期元素,由族序数等于周期数3倍,若A为第二周期,则位于第ⅥA族,即A为O;由周期数等于族序数3倍的元素,则B在第三周期第ⅠA族,则B为Na;由常温下气体单质为双原子分子.C的气态氢化物能使酚酞溶液变红色,则C为N;由第三周期金属元素,能和B的最高价氧化物对应的水化物NaOH溶液反应生成氢气,则D为Al,
(1)C为N,有2个电子层,最外层电子数为5,原子结构示意图为
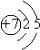
,故答案为:
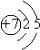
;
(2)Na、Al都在第三周期,从左向右金属性减弱,则Na的金属性强,可利用单质与水或与酸的反应,最高价氧化物对应水化物的碱性等来判断,故选②,
故答案为:Na;②;
(3)设原混合气体中的CO2质量为x,
由CO2+Na2O2═Na2CO3+O2△m
44 28
x 5.6gg
=44 x
,解得x=8.8g,28 5.6g
则原混合气体中的CO2质量分数为
×100%=88%,故答案为:88%;8.8g 10g
(4)向某无色透明的溶液中加入Al的粉末,反应后只生成氢气,则无色溶液可能为酸或碱的溶液,
A、无论酸或碱的溶液,该组离子之间不反应,则一定能大量共存,故A正确;
B、HCO3-既能与酸反应,又能与碱反应,则一定不能大量共存,故B错误;
C、碱性条件下不反应,但酸溶液中CO3-与氢离子反应,则可能共存,故C错误;
D、酸溶液中不反应,但碱溶液中Al3+、NH4+都能与氢氧根离子反应,则可能共存,故D错误;
故答案为:A.
