过硼酸钠是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中.以硼砂(主要成为Na2B4O7)为原料生产过硼酸钠晶体的主要流程如下:
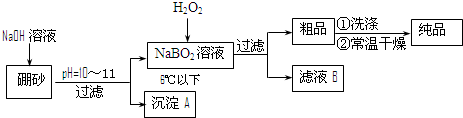
(1)由Na2B4O7和NaOH反应制NaBO2的离子方程式为______;
(2)沉淀A中含有酸不溶物和氢氧化镁杂质,为了分离出氢氧化镁,在沉淀中加过量的酸,过滤得到含Mg2+的滤液,再在滤液加入碱使Mg2+形成氢氧化镁.若加碱前溶液中c(Mg2+)=0.056mol•L-1,那么需调节溶液的pH=______时,才开始出现沉淀.[已知25℃下Mg(OH)2的Ksp=5.6×10-12]
(3)已知纯品过硼酸钠晶体中各元素的物质的量比为:n(Na):n(B):n(H):n(O)=1:1:n:7.将制得的纯品样品在
70℃以上加热将逐步失去结晶水,测得纯品质量随温度的变化如右图所示,则T3时所得晶体的化学式为______.(书写简单计算过程)

(4)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO2,则产品中钠的质量分数______(填“升高”、“降低”或“不变”).
(1)根据已知可写出反应物和部分生成物:
Na2B4O7+NaOH→NaBO2+?,根据质量守恒可知未知物为H2O,
配平后方程式为:Na2B4O7+2NaOH═4NaBO2+H2O,离子方程式为:
B4O72-+2OH-=4BO2-+H2O.
故答案为:B4O72-+2OH-=4BO2-+H2O.
(2)Mg2+沉淀的PH计算如下:Ksp═c(Mg2+)×c(OH-)2 ,设c(OH-)浓度为x,带入Ksp表达式得:
0.056×x2═5.6×10-12,解得x═1.0×10-5,C(H+)=1×10-14÷1.0×10-5═1×10-9,pH═9.故调节溶液的pH=9时,才开始出现沉淀.
故答案为:9.
(3)计算过程:T3时,nNa=(20.0g×23%)/23g.mol-1=0.2mol
则30.8g样品中,nNa:nB:nH:nO=0.2:0.2:0.2n:1.4
有:0.2×23+0.2×11+0.2n+1.4×16=30.8
解出n=8,则原晶体为:NaBO3•4H2O.
进一步根据T3时所得晶体中钠元素的质量分数,求出结晶水数目:23÷(23+11+48+18n)═0.23,解得n═1.
所以T3时所得晶体的化学式为NaBO3•H2O.
故答案为:NaBO3•H2O
(4)比较化学式NaBO3•H2O、NaBO2 可知,NaBO2 中钠的质量分数大于NaBO3•H2O 中钠的质量分数.所以过硼酸钠晶体中混有NaBO2,则产品中钠的质量分升高.
故答案为:升高.
