问题
选择题
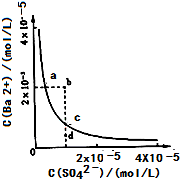
难溶物BaSO4在水中的溶解平衡可表示为:BaSO4(s)⇌Ba2+(aq)+SO42-(aq).其溶度积常数Ksp=C(Ba2+)•C(SO42-),某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
A.d点无BaSO4沉淀生成
B.加入Na2SO4可以使溶液由a点变到b点
C.通过蒸发可以使溶液由d点变到c点
D.a点对应的Ksp大于c点对应的Ksp
答案
A、d点表示Qc<Ksp,溶液不饱和,不会有沉淀析出,故A正确;
B、硫酸钡溶液中存在溶解平衡:BaSO4(s)⇌Ba2+(aq)+SO42-(aq),a点在平衡曲线上,加入Na2SO4,平衡左移,c(SO42-)增大,c(Ba2+)降低,故B错误;
C、d点时溶液不饱和,蒸发溶剂水,c(SO42-)、c(Ba2+)均增大,不可以使溶液由d点变到c点,故C错误;
D、Ksp是一常数,温度不变,Ksp不变,在曲线上的任意一点Ksp都相等,故D错误.
故选:A.
