工业上制氯化铜无水物时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁和SiO2),充分搅拌后使之溶解,制取流程如下:
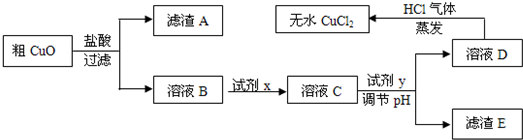
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38.试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH=______.
(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是______.
(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是______(填以下选项序号).
A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为______.
(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是______(填以下选项序号),原因是______.
A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是______.(NA表示阿伏伽德罗常数)
A.粗CuO中Cu2+数目小于
B.粗CuO中CuO物质的量小于 aNA 80
molb 135
C.粗CuO中所含的铜元素的质量分数为
x100%64b 135a
D.粗CuO中关于CuO的量无法确定.
(1)Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38 当溶液中的Fe3+完全沉淀,此时溶液中的Fe3+物质的量的浓度=10-5mol/L,c(Fe3+).c3(OH-)=1.0×10-38;c3(OH-)=10-33,c(OH-)=10-11mol/L,c(H+)=10-3mol/L,PH=3;
故答案为:3;
(2)溶液D是氯化铜溶液,制取无水CuCl2时,需在HCl气体中蒸干是防止氯化铜水解,HCl抑制CuCl2水解;
故答案为:HCl抑制CuCl2水解;
(3)粗CuO溶于过量盐酸后,得到的溶液B中含有氯化铜和氯化亚铁,加入试剂x将Fe2+氧化为Fe3+,试剂x可以氧化亚铁离子,但不能引入新的杂质;
A.KMnO4溶液 可以氧化亚铁离子但引入钾离子、锰离子,故A不符合;
B.氯水氧化亚铁离子为氯化铁,故B符合;
C.NaClO溶液氧化亚铁离子,引入钠离子,故C不符合;
D.O3氧化亚铁离子,不引入新的杂质,故D符合;
过氧化氢氧化亚铁离子为铁离子,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案为:BD; 2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)加入试剂和酸反应调节溶液PH使铁离子全部沉淀,加入的试剂不能引入新的杂质;溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是
A.NaOH溶液引入钠离子,故A符合;
B.Cu(OH)2固体可以调节溶液PH,不一如杂质,故B不符合;
C.Cu2(OH)2CO3固体可以调节溶液PH,不一如杂质,故C不符合;
D.CuO固体可以调节溶液PH,不一如杂质,故D不符合;
故答案为:A,将引入新杂质NaCl;
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),
A.粗CuO中含有其他物质,所以Cu2+数目小于
故A正确;aNA 80
B.粗CuO中含有其他物质,CuO物质的量小于
mol,故B正确;b 135
C.粗CuO中含有其他物质,所含的铜元素的质量分数小于
x100%,故C错误;64b 135a
D.粗CuO中杂质不能确定其治疗,关于CuO的量无法确定,故D正确;
故答案为:ABD.
