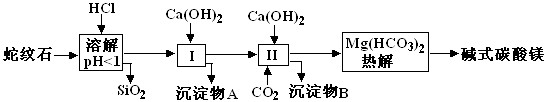
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致______溶解、______沉淀.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入______ (填入物质的化学式),然后______ (依次填写实验操作名称).
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是______(填写物质化学式).
(5)现设计一个实验,确定产品aMgCO3•bMg(OH)2•cH2O中a、b、c的值(已知均为正整数),请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):①样品称量 ②高温分解 ③______ ④______ ⑤称出MgO的质量.
(1)蛇纹石加盐酸溶解,MgO、Fe2O3、Al2O3和HCl反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O.而SiO2不与盐酸反应,以沉淀的形式除去,故答案为:Fe3+、Al3+;
(2)由(1)知,此时溶液中除了Mg2+外,还含有Fe3+、Al3+杂质,需除去Fe3+、Al3+但不能损失Mg2+,因Fe3++3H2O⇌Fe(OH)3+3H+和Al3++3H2O⇌Al(OH)3+3H+,利用平衡移动的原理,消耗H+使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,加Ca(OH)2需将溶液的pH控制在7~8,若pH过高,会导致生成的Al(OH)3发生反应Al(OH)3+OH-=AlO2-+2H2O溶解,Mg(OH)2在pH为9.4时开始沉淀,所以碱性增强Mg(OH)2会沉淀,同时Mg2+也因转化为沉淀而损失,
故答案为:Al(OH)3;Mg(OH)2;
(3)从实验步骤图知:沉淀混合物为Fe(OH)3和Al(OH)3,红色氧化物是沉淀物Fe(OH)3分解后得到的Fe2O3,所以得先加碱把Al(OH)3除掉,反应为:Al(OH)3+NaOH=NaAlO2+2H2O,然后过滤洗涤灼烧即可,故答案为:NaOH;过滤、洗涤、灼烧;
(4)从实验步骤图知:上述实验中,步骤Ⅱ中通二氧化碳,生成碳酸钙,碳酸钙分解可得到二氧化碳,作为第Ⅱ步的原料,碱式碳酸镁分解得到CO2,可以循环使用的物质是CaCO3或CO2,故答案为:CaCO3或CO2;
(5)利用浓硫酸的吸水性测出浓硫酸的增重测出水蒸汽的质量;利用碱石灰吸收CO2前后的质量差求二氧化碳质量,
故答案为:③测出水蒸汽的质量(或测出浓硫酸的增重);④测出CO2的质量(或测出碱石灰的增重).
