问题
填空题
“烂板液”是制印刷锌板时,用稀HNO3腐蚀锌板后得到的废液,主要含Zn(NO3)2和由自来水带进的Cl-、Fe3+等杂质离子.在实验室中由“烂板液”制取ZnSO4•7H2O的过程如下:
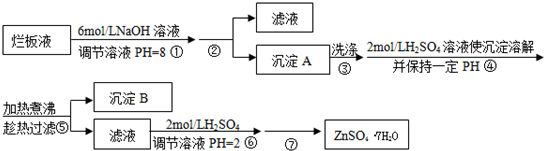
已知有关金属离子形成氢氧化物沉淀时的PH见下表:
| 离子 | 开始沉淀时的PH | 完全沉淀时的PH |
| Fe3+ | 1.9 | 3.2 |
| Zn2+ | 6.4 | 8.0 |
(2)第②步操作中需要的玻璃仪器有______.
(3)第④步中PH应保持在______.
(4)第⑥步调节溶液PH=2的目的是______.
(5)操作⑦包含3个基本实验操作,它们是______、______和过滤.
答案
(1)用SCN-检验Fe3+是否有剩余,故答案为:取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe(OH)3 沉淀完全;
(2)过滤需要用到玻璃仪器有漏斗、玻璃棒、烧杯,故答案为:漏斗、玻璃棒、烧杯;
(3)第④步目的是使Fe3+完全沉淀,Zn2+不沉淀故应调节PH为3.2~6.4,故答案为:3.2~6.4;
(4)锌离子易水解生成氢氧化锌,酸性条件下可抑制锌离子的水解,故答案为:抑制Zn2+水解;
(5)操作⑦包括蒸发浓缩,冷却结晶,过滤,故答案为:蒸发浓缩;冷却结晶(或降温结晶).
