难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如:Cu(OH)2
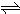
Cu2++2OH-,Ksp=c(Cu2+)•[c(OH-)]2=2×10-20.当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
(1)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于______.
(2)要使0.2mol•L-1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为______.
(1)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,则应有c(OH-)≥
mol/L=10-9mol/L,则c(H+)≤2×10-20 0.02
mol/L=10-5mol/L,1×10-14 10-9
所以pH≥-lg(10-5)=5,故答案为:5;
(2)Cu2+沉淀较为完全是的浓度为
=2×10-4mol/L,0.2mol/L 1000
则c(OH-)=
mol/L═108mol/L,2×10-20 2×10-4
则c(H+)=
mol/L=10-6mol/L,1×10-14 10-8
所以pH=-lg(10-6)=6,
故答案为:6.
