七水硫酸镁(MgSO4•7H2O)在印染、造纸和医药等工业上都有广泛的应用.可利用化工厂生产硼砂的废渣M(主要成分是MgCO3,还含有MgO、SiO2、Fe2O3、FeO、CaO、Al2O3等杂质)来制取七水硫酸镁.已知:
表1 部分阳离子以氢氧化物形式完全沉淀时的pH
| 沉淀 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度 | 10℃ | 30℃ | 40℃ | 50℃ | 60℃ |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4•7H2O | 30.9 | 35.5 | 40.8 | 45.6 | -- |
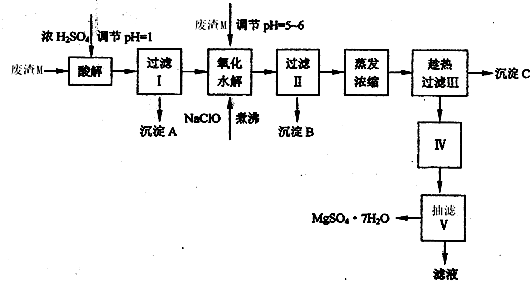
回答下列问题:
(1)过滤I的滤液中加入NaClO溶液的目的是______,写出反应的离子方程式______,需要加热煮沸的目的是______.
(2)操作Ⅱ所用的玻璃仪器是______.
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+,其实验方法是______.(用离子方程式表示).
(4)沉淀C的化学式是______,过滤Ⅲ需趁热过滤的理由是______.
(1)根据表中数据可知Fe3+易水解生成Fe(OH)3沉淀,NaClO具有氧化性,能将Fe2+氧化为Fe3+,易于除杂,
反应的方程式为6Fe2++3ClO-+3H2O=2Fe(OH)3↓+4Fe3++3Cl-或2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,
盐的水解为吸热过程,加热有利于促进Al3+、Fe3+的水解生成Fe(OH)3、Al(OH)3等沉淀,
故答案为:将Fe2+氧化为Fe3+;6Fe2++3ClO-+3H2O=2Fe(OH)3↓+4Fe3++3Cl-或2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;促进Al3+、Fe3+的水解;
(2)过滤用到的仪器或用品有铁架台(带铁圈)、烧杯、玻璃棒、漏斗以及滤纸,其中玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:烧杯、漏斗、玻璃棒;
(3)实验室检验Fe3+离子的方法是在溶液中加入KSCN,溶液变红色,反应的离子方程式为Fe3++3SCN-=Fe(SCN)3,
故答案为:Fe3++3SCN-=Fe(SCN)3;
(4)趁热过滤时,硫酸钙的溶解度较小,而硫酸镁的溶解度较大,易于分离混合物,
此时过滤得到的沉淀为CaSO4•2H2O或CaSO4,如不趁热过滤,冷却后硫酸镁的溶解度减小,会生成硫酸镁晶体,
故答案为:CaSO4•2H2O或CaSO4;防止MgSO4在温度降低时结晶析出.
