常温下,2.0×10-3mol•L-1氢氟酸的水溶液中,调节溶液pH(忽略溶液体积变化)得到的[HF]、[F-]与溶液pH的变化关系如下图.下列叙述不正确的是( )
(提示:Ka(CH3COOH)=1.8×10-5mol•L-1,Ksp(CaF2)=1.5×10-10mol3•L-3)
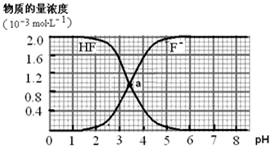
A.两条曲线交点a对应溶液的[F-]=[HF]
B.加入NaOH溶液至pH=7,溶液中[F-]=[Na+]
C.常温下HF的电离常数Ka(HF)>Ka(CH3COOH)
D.pH=4时,加入CaCl2固体使[Ca2+]=2.0×10-3mol•L-1,无CaF2沉淀析出
A、纵轴是微粒浓度,横轴是溶液PH,两条曲线交点a对应溶液的[F-]=[HF],故A正确;
B、加入NaOH溶液反应HF+NaOH=NaF+H2O;溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(F-),至pH=7,c(H+)=c(OH-),溶液中[F-]=[Na+],故B正确;
C、Ka=
;当c(F-)=C(HF)时,Ka=c(H+)=10-3.5=3.5×10-4mol•L-1>Ka(CH3COOH)=1.8×10-5mol•L-1,常温下HF的电离常数Ka(HF)>Ka(CH3COOH),故C正确;c(H+)c(F-) c(HF)
D、分析图象当PH=4.0,溶液中的F-离子浓度1.6×10-3mol;加入CaCl2固体使c(Ca2+)=2.0×10-3mol•L-1,c(Ca2+)×c2(F-)=2.0×10-3mol•L-1×(1.6×10-3)2=5.1×10-10>Ksp(CaF2),有沉淀生成,故D错误;
故选D.
