问题
选择题
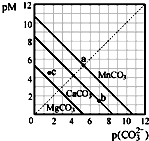
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),pc(CO32-)=-lgc(CO32-).下列说法正确的是( )
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32-)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-)
答案
A.pM相等时,图线中p(CO32-)数值越大,实际浓度越小,因此,MgCO3、CaCO3、MnCO3的Ksp依次减小,故A错误;
B.a点可表示MnCO3的饱和溶液,pM=p(CO32-),所以c(Mn2+)=c(CO32-),故B正确;
C.b点可表示CaCO3的饱和溶液,pM<p(CO32-),所以c(Ca2+)>c(CO32-),故C错误;
D.pM数值越小,实际浓度越大,已知c点不在曲线上,而在曲线下面,则c点表示MgCO3的过饱和溶液,pM>p(CO32-),所以c(Mg2+)<c(CO32-),故D错误;
故选:B.
