问题
计算题
(3分)常温下,FeS的Ksp=6.25×10-18(设饱和溶液的密度为1g/mL)。若已知H2S饱和溶液在常温下,c(H+)与c(S2-)之间存在以下关系:c2(H+)·c(S2-)=1.0×10-22,在该温度下,将适量FeS投入H2S饱和溶液中,欲使溶液中c(Fe 2+)达到1mol/L,应调节溶液的pH为
(已知:lg2 = 0.3)
答案
pH=3-2lg2= 2.4
考查溶度积常数的有关计算。c(Fe 2+)达到1mol/L,则根据FeS的Ksp=6.25×10-18可知硫离子的浓度为c(S2-)=6.25×10-18mol/L。又因为c2(H+)·c(S2-)=1.0×10-22,所以c(H+)=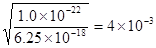 ,所以pH=3-2lg2= 2.4。
,所以pH=3-2lg2= 2.4。
