(8分)对可逆反应aA(g)+bB(g)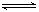 cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: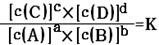 (为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)
(为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)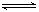 CO2(g)+H2(g),△H<0。在850℃时,K=1。
CO2(g)+H2(g),△H<0。在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K 1(填“大于”、“小于”或“等于”)。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2和x mol H2,则:①当x=5.0时,上述平衡向 (填“正反应”或“逆反应”)方向移动。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是 。
(3)在850℃时,若设x=5.0和x=6.0,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a b(填“大于”、“小于”或“等于”)。
(1)小于 (2)①逆反应 ②x<3.0 (3)小于
题目分析:(1)CO(g)+H2O(g)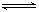 CO2(g)+H2(g),△H<0。反应放热。根据勒夏特列原理,升温平衡向吸热反应方向移动。对该反应而言即为左移。化学平衡常数K减小。填 “小于”。① 根据化学平衡常数K表达式与QC表达式的关系。QC大于K平衡向逆反应方向移动。②QC小于K平衡向正反应方向移动。求得x<3.0符合题意。其他物质的投料不变H2投料越多其转化率越低。K表达式与QC表达式的关系,勒夏特列原理等高考高频考点
CO2(g)+H2(g),△H<0。反应放热。根据勒夏特列原理,升温平衡向吸热反应方向移动。对该反应而言即为左移。化学平衡常数K减小。填 “小于”。① 根据化学平衡常数K表达式与QC表达式的关系。QC大于K平衡向逆反应方向移动。②QC小于K平衡向正反应方向移动。求得x<3.0符合题意。其他物质的投料不变H2投料越多其转化率越低。K表达式与QC表达式的关系,勒夏特列原理等高考高频考点
点评:该题考查化学平衡常数K表达式与QC表达式的关系,勒夏特列原理等高考高频考点。
