问题
选择题
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol •L-1,向该溶液中逐滴加入0.010 mol •L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 ( )
A.Cl-、Br-、CrO42-
B.CrO42-、Br-、Cl-
C.Br-、Cl-、CrO42-
D.Br-、CrO42-、Cl-
答案
答案:C
在一定温度下,在难溶化合物的饱和溶液中组成沉淀的各离子的浓度的乘积是一常数,称溶度积常数。运用Ksp的公式进行计算,只要注意到AgCl、AgBr和Ag2CrO4的Ksp表达式不同,计算银离子的浓度即可。
c(Ag+)=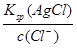 =
=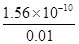 = 1.56×10-8
= 1.56×10-8
c(Ag+)=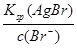 =
= = 7.7×10-11
= 7.7×10-11
c(Ag+)=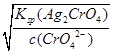 =
=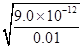 =3.0×10-5
=3.0×10-5
根据计算可知,三种离子产生沉淀的先后顺序为Br-、Cl-、CrO42-,选项C正确。
【考点定位】沉淀溶解平衡、溶度积常数
