AgCl(s)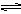 Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为
Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为
A.③①②④
B.④①②③
C.①②③④
D.④③②①
答案:B
题目分析:从平衡移动的角度分析,将过量氯化银分别放入下列溶液中,依据温度不变
Ksp=c(Ag+)•c(Cl-)为定值,Cl-浓度越大,则Ag+的浓度越小;①100mL蒸馏水中,c(Cl-)=0,②24mL 0.1mol•L-1NaCl,c(Cl-)=0.1mol•L-1,③10mL 0.1mol•L-1MgCl2 中,c(Cl-)=0.2mol•L-1所以Cl-浓度:③>②>①,依据Ksp=c(Ag+)•c(Cl-)为定值,银离子浓度由大到小的顺序是:①②③,而④加入的是银离子,所以30mL 0.1mol•L-1AgNO3溶液中c(Ag+)=0.1mol•L-1,所以④中c(Ag+)最大;银离子浓度由大到小的顺序是:④①②③;选B。
