问题
选择题
向10 mL含等浓度的I-和Cl-的溶液中逐滴加入0.1 mol·L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。下列说法不正确的是
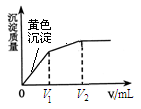
A.该实验可以证明AgI比AgCl更难溶
B.加入V2 mL AgNO3溶液后,溶液中不含I-
C.V1= V2-V1
D.向最终的沉淀中加入Na2S溶液,沉淀变成黑色
答案
答案:B
题目分析:A、AgNO3溶液与I-和Cl-均可产生AgI和AgCl沉淀,但直接生成黄色AgI沉淀,说明AgI溶解度更小,更难溶,故A正确;B、AgI是难溶电解质,难溶电解质放入水中会发生极少量的电离使溶液中有少量I-,故B错误;C、溶液中I-和Cl-的物质的量相等,即反应需要的银离子物质的量相等,V1= V2-V1,故C正确;D、因为Ag2S的溶解度比AgI小得多,所以发生沉淀的转化,生成溶解度更小的Ag2S黑色沉淀,故D正确。
