重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO•Cr2O3,杂质主要是二氧化硅和氧化铝)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:
6FeO•Cr2O3+24NaOH+7KClO3
12Na2CrO4+3Fe2O3+7KCl+12H2O △ .
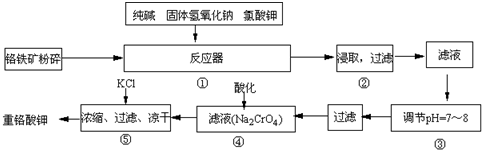
试回答下列问题
(1)指出24Cr在周期表中的位置是______,
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:______.
(3)操作③调节pH=7~8的原因是______.(用简要的文字和离子方程式说明)
下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系:
| pH | C(CrO42-)mol/L | C(HCrO4-)mol/L | C(Cr2O72-)mol/L | C(H2CrO4)mol/L |
| 4 | 0.0003 | 0.104 | 0.448 | 0 |
| 5 | 0.0033 | 0.103 | 0.447 | 0 |
| 6 | 0.0319 | 0.0999 | 0.437 | 0 |
| 7 | 0.2745 | 0.086 | 0.3195 | 0 |
| 8 | 0.902 | 0.0282 | 0.0347 | 0 |
| 9 | 0.996 | 0.0031 | 0.0004 | 0 |
(5)在铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2______K3(填>、﹦、<)
(6)上表中铬酸的物质的量浓度为______.(精确到小数点后2位)
(1)K元素原子序数为19,处于第四周期第1列,第四周期容纳18种元素,24Cr的原子序数比K元素大5,所以24Cr处于周期表中第四周期,第6列,故24Cr处于周期表中第四周期第ⅥB族.
故答案为:第四周期第ⅥB.
(2)NaFeO2水解生成Fe(OH)3与NaOH,反应方程式为NaFeO2+2H2O=Fe(OH)3↓+NaOH.
(3)由于溶液在硅酸钠和偏铝酸钠发生水解,SiO32-+H2O⇌HSiO3-+OH-,HSiO3-+H2O⇌H2SiO3+OH-,AlO2-+H2O⇌Al(OH)3+OH-,降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全.
故答案为:由于溶液在硅酸钠和偏铝酸钠发生水解,SiO32-+H2O⇌HSiO3-+OH-,HSiO3-+H2O⇌H2SiO3+OH-,AlO2-+H2O⇌Al(OH)3+OH-,降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全.
(4)由表中数据可知,铬酸(H2CrO4)溶液中pH越小,浓度越大Cr2O72-,加酸酸化使CrO42-转化为Cr2O72-.
故答案为:酸化使CrO42-转化为Cr2O72-.
(5)由表中数据可知,酸性条件下,铬酸(H2CrO4)溶液中Cr2O72-浓度远大于CrO42-.所以电离出CrO42-的电离平衡常数小于电离出Cr2O72-的电离平衡常数,即K2<K3.
故答案为:<.
(6)选择第1组计算.根据铬元素守恒可知c(H2CrO4)=c(CrO42-)mol/L+c(HCrO4-)mol/L+2c(Cr2O72-)mol/L=0.0003mol/L+0.104mol/L+2×0.448mol/L=1.0003mol/L≈1.00mol/L.
故答案为:1.00mol/L.
