常温下,向25 mL 0.1 mol/L MOH溶液中逐滴加入0.2 mol/L HA溶液,曲线如图所示(体积变化忽略不计)。回答下列问题

(1)写出MOH的电离方程式_________________________
(2)MOH与HA恰好完全反应时,溶液呈_____性(填“酸”、“碱”或“中”),理由是(用离子方程式表示)___________________;此时,混合溶液中由水电离出的c(H+)_____ 0.2 mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”)。
(3)分别写出B、C两点,混合溶液中各离子浓度的大小关系
B点______________;C点_____________;
(4)D点时,溶液中c(A-)+c(HA)________2c(M+)(填“>”“<”或“=”);若此时测得混合溶液的
pH=3,则c(HA) + c(H+) = __________mol/L。
(1)MOH==M++OH-
(2)碱;A- + H2O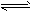 HA + OH-;>
HA + OH-;>
(3)c(M+) = c(A-)>c(H+) = c(OH-) ;c(A-)>c(M+)>c(H+)>c(OH-)
(4)=;0.05
