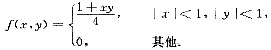问题
选择题
已知.25℃时有关弱酸的电离平衡常数如下表
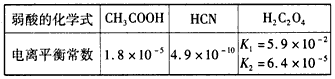
下列有关说法正确的是 [ ]
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)> pH(Na2C2O4)>pH(CH3COONa)
B.a mol/LHCN溶液与b mol/LNaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则b一定大于a
C.向冰醋酸溶液中逐滴加水,则溶液的导电性、醋酸的电离度、溶液的pH均先增大后减小
D.等物质的量的NaHC2O4和Na2C2O4的混合溶液中,一定存在:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
+2c(C2O42-)
答案
答案:D