(Ⅰ)(6分)现有下列物质: ①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)在上述状态下能导电的物质是 ;
(2)属于弱电解质的是 ;
(3)属于非电解质,但溶于水后的水溶液能导电的是 ;
(Ⅱ)(4分)
某化学实验小组探究市售食用白醋中醋酸的的准确浓度,取25.00mL某品牌食用白
醋于锥形瓶中,在实验室用浓度为cb mol/L的标准NaOH溶液对其进行滴定。
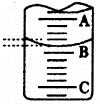
(1)左图表示50mL滴定管中液面的位置,若A与C刻度间相差l mL,
A处的刻度为25,滴定管中液面读数应为 mL。
(2)为了减小实验误差,该同学一共进行了三次实验,假设每次
所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实
验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
其原因可能是 。
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
C.第一次滴定用的锥形瓶未润洗
D.滴定结束时,俯视读数
(3)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):
c= 。
(Ⅲ)(15分)
已知:在25时H2O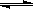 H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH 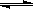 H++ CH3COO- Ka=1.8×10-5
H++ CH3COO- Ka=1.8×10-5
(1)取适量醋酸溶液,加入少量醋酸钠固体,此时溶液中C(H+)与C(CH3COOH)
的比值 (填“增大”或“减小”或“不变”)
(2)醋酸钠水解的离子方程式为 。当升高温度时,C(OH—)将
(填“增大”“减小”“不变”);
(3)0.5mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠
的比值)为a;1mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系
为 ,a与b的关系为 (填“大于”“小于”“等于”);
(4)将等体积等浓度的醋酸和氢氧化钠溶液混合后,所得溶液中离子浓度由大到小的顺序是 。
(5)若醋酸和氢氧化钠溶液混合后pH<7,则c(Na+)_______________ c(CH3COO-)(填“大于”、“小于”或“等于”),
(6)若由pH=3的HA溶液V1mL与pH=11的NaOH{溶液V2 mL。混合而得,则下列说法不正确的是____________。
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(7)在某溶液中含Mg2+、Cd2+、Zn2+三种离子的浓度均为0.01mol·L-1。向其中加入固
体醋酸钠后测得溶液的C(OH-)为2.2×10-5mol·L-1,以上三种金属离子中
能生成沉淀,原因是
(KSP[Mg(OH)2]=1.8×10-11、KSP[Zn(OH)2]=1.2×10-17、KSP[Cd(OH)2]=2.5×10-14)
(8)取10mL0.5mol·L-1盐酸溶液,加水稀释到500mL,则该溶液中由水电离出的c(H+)
= 。
(Ⅰ)⑤⑦⑧;③;②;(每空2分)
(Ⅱ)
(1)25.40 mL(1分)
(2)A、B(2分)
(3)C(25.35+25.30)/25.00(1分)
(Ⅲ)(1)减小(1分)
(2)CH3COO— + H2O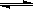 CH3COOH+OH-;增大(3分)
CH3COOH+OH-;增大(3分)
(3)小于;大于(2分)
(4)c(Na+)>c(CH3COO-)>c(OH-)>c(H+)(2分)
(5)大于(1分)
(6)AD(2分)
(7)Cd2+、Zn2+;(1分)
[OH-]=2.2×10-5mol·L-1
[M2+][OH-]2=5×10-12(mol·L-1)3
5×10-12小于KSP[Mg(OH)2]=1.8×10-11
5×10-12大于KSP[Zn(OH)2]=1.2×10-17
5×10-12大于KSP[Cd(OH)2]=2.5×10-14(2分)
(8)1×10-12
该题考查的是电解质溶液,包含它的电离与水解,这部分内容的题较难,它的难在于弱电解质、水解及沉淀溶解都是可逆的,所以它涉及到化学平衡方面的内容,考查范围较广。
(Ⅰ)、(Ⅱ)较简单,这里不再赘述,不过我认为(Ⅱ)第3小题的答案有误,答案应该是
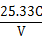
(Ⅲ)
(1) 醋酸溶液中存在电离平衡:CH3COOH 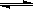 H++ CH3COO-,当加入醋酸钠固体时,CH3COO-浓度上升,平衡向左移动,导致结果就是C(H+)减小,C(CH3COOH)增大,所以C(H+)与C(CH3COOH)的比值减小。
H++ CH3COO-,当加入醋酸钠固体时,CH3COO-浓度上升,平衡向左移动,导致结果就是C(H+)减小,C(CH3COOH)增大,所以C(H+)与C(CH3COOH)的比值减小。
(2) CH3COO— + H2O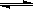 CH3COOH+OH-,水解是吸热的,当温度升高是平衡向右移动,所以C(OH—)升高
CH3COOH+OH-,水解是吸热的,当温度升高是平衡向右移动,所以C(OH—)升高
(3) 醋酸钠溶液存在水解平衡:CH3COO— + H2O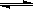 CH3COOH+OH-,1mol·L-1醋酸钠溶液相当于在0.5mol·L-1基础上加入醋酸钠,水解平衡向右移动,C(OH—) 升高,所以m<n,但这种化学平衡只能抑制醋酸钠加入的影响,而不能抵消,根据水解度的定义,所以a>b。
CH3COOH+OH-,1mol·L-1醋酸钠溶液相当于在0.5mol·L-1基础上加入醋酸钠,水解平衡向右移动,C(OH—) 升高,所以m<n,但这种化学平衡只能抑制醋酸钠加入的影响,而不能抵消,根据水解度的定义,所以a>b。
(4) 等体积等浓度的醋酸和氢氧化钠溶液混合生成醋酸钠,呈碱性,所以C(Na+)>C(CH3COO—)> C(OH—)> C(H+)(溶液中存在电荷守恒)
(5) 根据电荷守恒,C(OH—)<C(H+),必然有C(Na+)<C(CH3COO—)
(6) 本人觉得这道题答案有误,正确答案应该是B、C。如果等体积混合pH=3的HA溶液与pH=11的NaOH,溶液pH<7,这是因为醋酸是弱电解质,醋酸分子会在混合过程中电离出H+,所以B、C说法不正确。
(7) (8)简单
