问题
填空题
(14分)、根据电离平衡移动原理完成下列表格
(1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况
| 外加条件 | 平衡移动方向 | C(OH -) | C(CH3COO -) |
| 升温 | 不填 | 不填 | |
| 加水 | 不填 | ||
| 加盐酸 | 不填 | ||
| 加少量氢氧化钠固体 | 不填 | 不填 |
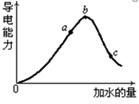
①写出醋酸的电离方程式________________。
②a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
③a、b、c三点中醋酸的电离程度最大的是 。
④取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲_____ 10C(H+)乙(填“大于”、“小于”或 “等于”),
答案
(14分)、
(1)(每空1分)
| 外加条件 | 平衡移动方向 | C(OH -) | C(CH3COO -) |
| 升温 | 正向移动 | ||
| 加水 | 正向移动 | 增大 | |
| 加盐酸 | 减小 | 减小 | |
| 加少量氢氧化钠固体 | 增大 |
①_ CH3COOH CH3COO + H+ 。
CH3COO + H+ 。
②__b>a>c__ 。
③ c 。
④C(H+)甲___小于 __ 10C(H+)乙
