(2011年湖南怀化,31题)根据右图浓盐酸的商标,回答下列问题

(1)某研究小组的同学欲用该盐酸配制100g10%的稀盐酸,需该盐酸 g(保留一位小数),配制时应选用 (填“10ml”或“50ml”)量筒量取。
(2)小组同学用所配制稀盐酸来测量水垢【主要成分为CaCO3和Mg(OH)2】中CaCO3的质量分数:取10.0g水垢,加入所配100g10%的稀盐酸中,测得各时间段内生成气体的质量如下表:
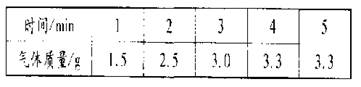
通过实验,计算该水垢中CaCO3的质量分数。
(1)27.0 50ml
(2)解:设该水垢中CaCO3的质量为x
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
44
x 3.3g
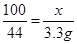
x=7.5g
该水垢中CaCO3的质量分数为: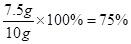
答:该水垢中CaCO3的质量分数为75%。
分析:(1)根据稀释时溶质的量不变计算盐酸的质量,并求出体积,选择所需量筒;
(2)根据已有的知识进行分析,碳酸钙能与盐酸反应生成二氧化碳,而氢氧化镁与盐酸反应生成的时氯化镁和水,不生成气体,根据表格提供的数据即可求得碳酸钙的质量,从而求得碳酸钙的含量.
解答:解:(1)根据浓溶液质量×浓溶液的质量分数=稀溶液质量×稀溶液的质量分数,
所需盐酸质量=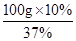 =27.0g,体积为27.0g÷1.18g/cm3=23cm3=23mL,选用50mL的量筒;
=27.0g,体积为27.0g÷1.18g/cm3=23cm3=23mL,选用50mL的量筒;
(2)无论10g的样品是纯的碳酸钙还是氢氧化镁,完全反应需要的盐酸都不超过10g,所以盐酸是过量的.碳酸钙能与盐酸反应生成二氧化碳,而氢氧化镁与盐酸反应不生成二氧化碳,当气体质量不再改变,说明碳酸钙已经反应完全,所以4分钟后反应已完全;
设生成3.3g二氧化碳需要碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 3.3g

x=7.5g
该水垢中CaCO3的质量分数为:
| 7.5g |
| 10.0g |
答:(1)27.0,50mL;
(2)答:该水垢中CaCO3的质量分数为75%.
