问题
计算题
【10新疆21】.(4分)实验室有一瓶标签已破损的过氧化氢溶液,同学们为了测定瓶内溶液的溶质质量分数,他们取该溶液34g于烧杯中,加入3gMnO2完全反应后,称得烧杯内剩余物质的总质量为33.8g,请你和他们一起计算:
(1)反应后生成氧气的质量是多少?
(2)所取溶液中溶质的质量是多少?
(3)该瓶过氧化氢溶液的溶质质量分数是多少?
答案
(1)3.2g(2)6.8g(3)20℅
本题考查的是根据化学反应方程式的计算;有关溶质质量分数的简单计算。
(1).
(2)可根据求出氧气的质量,利用过氧化氢分解的化学方程式,求出过氧化氢的质量,再进一步求出质量分数.解答:
(1)可根据质量守恒定律求出反应前后烧杯中物质的质量差,就是生成氧气的质量,生成氧气质量即为反应前后烧杯中物质的质量之差,(34g+3g)-33.8g=3.2g
(2)设反应前溶液中含溶质过氧化氢质量为x
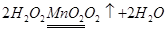
68 32
x 3.2g
68/x ="32/3.2g"
解之得:x=6.8g
过氧化氢溶液中溶质质量分数="6.8g/34g" ×100%=20%
答:生成氧气的质量是3.2g,所取溶液中溶质的质量是6.8g,瓶内过氧化氢溶液中溶质的质量分数为20%。
