问题
计算题
(3分)纯碱其主要成分是Na2CO3,是日常生活中常用的一种食品添加剂,青海湖的水中含有大量的Na2CO3,通过结晶的方法可以制得纯碱,但其中中往往含有杂质NaCl,为测定某纯碱产品的纯度进行了如下操作:
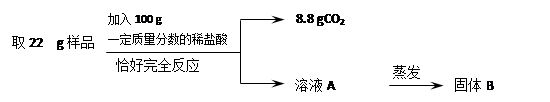
提示:上述实验中发生的化学反应是:Na2CO3+ 2HCl=2NaCl + H2O+ CO2↑
试求出(1)此纯碱样品的纯度
(2)溶液A中的溶质质量分数
答案
(1)求出碳酸钠的质量21.2克-------------1分
(2)求出样品纯度:96.4%--------------1分
(3)求出A的质量分数21.4%--------------1分
解:设样品中碳酸钠的质量为x,生成的氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
X Y 8.8g
106:44=X:8.8g
X=21.2g
117:44= Y:8.8g
Y=23.4g
此纯碱的纯度为:21.2/22×100%=96.4%
样品中有氯化钠22-21.2=0.8g
故溶液中氯化钠的质量为:0.8g+23.4g=24.2g
溶液质量为:22+100-8.8=113.2g
故溶液A中的溶质质量分数为:24.2/113.2×100%=21.4%
答:此纯碱样品的纯度是96.4%,溶液A中的溶质质量分数为21.4%.
