(7分)化石燃料的燃烧、硫酸的生产都产生二氧化硫,被雨水吸收后会形成酸雨,使农作物、建筑物等遭到破坏。
(1)通过测定雨水的 来粗略判断其是否为酸雨。
(2)环保部门能较为精确测定某硫酸厂周围空气中二氧化硫的含量。取空气样品1000m3缓缓通过足量氯水(化学方程式:SO2+Cl2+2H2O=2HCl+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生的白色沉淀质量为2.33g。
试回答:
①二氧化硫中硫元素与氧元素的质量比为 ;
②配制氯化钡溶液时,需用到的玻璃仪器有烧杯、量筒和 。
③上述实验中加入过量的氯化钡溶液的目的 。
④我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如右表所示,请通过计算说明此空气中二氧化硫的浓度级别。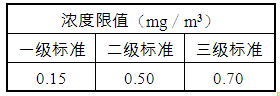
(1) PH值 (2)①1:1 ②玻璃棒 ③使硫酸完全反应
④SO2的浓度:0.64g/1000m3=0.64mg/m3>0.50mg/m3,为三级标准。
(1)可用pH试纸测定酸雨的酸碱度
(2)根据化学式可计算出二氧化硫中硫元素与氧元素的质量比,配制一定质量分数的溶液用到的仪器有:天平、烧杯、量筒、玻璃棒进行解答
(4)根据反应的化学方程式,由白色沉淀硫酸钡的质量计算出1000m3空气中所含二氧化硫的质量,转化为标准表示法mg/m3,与级别标准对比,判断出空气中二氧化硫的浓度级别
④解:设溶液中H2SO4的质量为x
H2SO4+BaCl2 = BaSO4↓+2HCl
98 233
x 2.33g
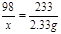 x=0.98g (1分)
x=0.98g (1分)
设1000m3空气样品中SO2的质量为y
SO2+Cl2+2H2O=2HCl+H2SO4
64 98
y 0.98g
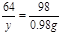 y=0.64g (1分)
y=0.64g (1分)
SO2的浓度:0.64g/1000m3=0.64mg/m3>0.50mg/m3,为三级标准。(1分)
