(6分) 某地一辆满载浓硫酸的罐车翻倒,导致25t溶质质量分数为98%的浓硫酸泄漏,并向路基两边蔓延,接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)25t溶质质量分数为98%的浓硫酸中含H2SO4的质量为 ;(2分)
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙;(写出计算过程,2分)
(3)处理一定量的硫酸,理论上既可用m1吨的氢氧化钙粉末,也可选用m2吨的氧化钙粉末,还可用m3吨碳酸钙粉末,则m1、m2、m3的数值大小关系为 。(2分)
(1) 24.5t (2)18.5t (3) m3>m1>m2
(1)溶质的质量=溶液的质量×溶质质量分数=25t×98%=24.5t。
(2)利用化学方程式计算可得出氢氧化钙的质量。
解:设理论上需要氢氧化钙的质量为x
H2SO4 + Ca(OH)2 ="==" CaSO4 + 2H2O
98 74
24.5t x
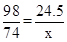 x=18.5t
x=18.5t
(3)利用化学方程式分别计算出m1、m2、m3的数值,然后比较大小关系。
H2SO4+ Ca(OH)2 ="==" CaSO4 + 2H2O H2SO4+ CaO="==" CaSO4 + H2O
98 74 98 56
24.5t m1 24.5t m2
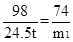
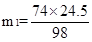
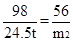
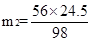
H2SO4+ CaCO3 ="==" CaSO4 + H2O + CO2↑
98 100
24.5t m3
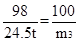
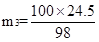
故:m3>m1>m2




