(15分)(Ⅰ)在温度t ℃时,pH=3的某水溶液中c(OH-)=10-9 mol/L在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为__________。
(Ⅱ)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性,生成的盐化学式为___________。AOH与HnB完全中和所得溶液呈_________性,其原因用离子方程式表_______________________________________。
(Ⅲ)常温下将体积为v1、浓度为c1的一元酸HA与体积为v2、浓度为c2的一元碱BOH混合。
(1)若v1·c1=v2·c2,混合后的溶液pH>7,则一元弱酸的电离程度 (选填“>”、“<”或“=”)一元弱碱的电离程度;
(2)若v1=v2,一元弱碱的电离程度大于一元弱酸的电离程度,且混合后溶液pH<7,则c1 c2(选填“>”、“<”或“=”)。
(Ⅳ)常温下,0.1m01/L的下列溶液:
①HCl、②CH3COOH、③CH3COONa、④NaOH、⑤FeCl3、⑥NaCl。
(1)pH由小到大排列顺序为 (填序号);
(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
(Ⅴ)将硫酸铝溶液和碳酸氢钠溶液混合时,可看到的实验现象是 ,产生该现象的原因是 (用离子方程式解释原因)。
(15分)(Ⅰ)10-4 (2分)
(Ⅱ)AnB (1分) 碱(1分) Bn-+H2O B(n-1)- + OH-(2分)
B(n-1)- + OH-(2分)
(Ⅲ)(1)<(1分) (2) >(1分)
(Ⅳ)(1)①②⑤⑥③④(2分) (2)Fe3++3H2O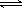 Fe(OH)3+3H+(2分)
Fe(OH)3+3H+(2分)
(Ⅴ)产生白色沉淀同时产生无色气体(1分)Al3+ +3HCO3— ==3CO2↑ +Al(OH)3↓(2分)
题目分析:(Ⅰ)pH=3的某水溶液中c(OH-)=10-9 mol/L,这说明该温度下水的离子积常数等于10-12。在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为10-8︰10-4=10-4。
(Ⅱ)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性,这说明酸一定是过量的,因此酸是弱酸,生成的盐化学式为AnB。由于酸是弱酸,所以生成的盐水解溶液显碱性,水解方程式是Bn-+H2O B(n-1)- + OH-。
B(n-1)- + OH-。
(Ⅲ)(1)若v1·c1=v2·c2,混合后的溶液pH>7,说明溶液显碱性,因此一元弱酸的电离程度小于一元弱碱的电离程度。
(2)若v1=v2,一元弱碱的电离程度大于一元弱酸的电离程度,且混合后溶液pH<7,这说明酸一定是过量的,所以则c1>c2。
(Ⅳ)(1)盐酸是一元强酸,醋酸是一元弱酸,而氢氧化钠是强碱。根据水解的规律可知,溶液中pH由小到大排列顺序为①②⑤⑥③④。
(2)由于氯化铁溶于水水解,方程式为Fe3++3H2O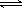 Fe(OH)3+3H+,所以有可能生成氢氧化铁沉淀而变混浊。
Fe(OH)3+3H+,所以有可能生成氢氧化铁沉淀而变混浊。
(Ⅴ)硫酸铝水解溶液显酸性,碳酸氢钠水解溶液显碱性,二者混合相互促进,所以可以产生白色沉淀同时产生无色气体,方程式是Al3+ +3HCO3— ==3CO2↑ +Al(OH)3↓。
点评:判断溶液的酸碱性时,需要依据氢离子浓度和OH-浓度的相对大小进行。如果是酸碱中和后溶液酸碱性的判断,则需要首先进行酸碱的过量判断,然后才能再考虑盐类的水解。
