某课外研究小组,用含有较多杂质的铜(主要杂质为Fe),通过下列化学反应制取胆矾。请回答相关问题:
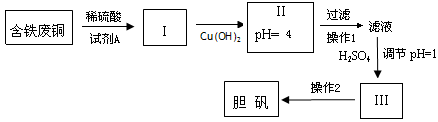
pH控制可参考下列数据:
| 物 质 | 开始沉淀时的pH | 完全沉淀时的pH |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
a. H2O2 b.氯水 c.酸性高锰酸钾
(2)Cu(OH)2的作用是 ,还可以用 (填一种试剂)代替;
(3)操作2包含3个基本实验操作,依次为 、 和过滤;
(4)某兴趣小组在对实验得到的胆矾进行结晶水实验的测定,小组成员经过讨论,采用以下方案:先对一定质量的胆矾灼烧失水,将加热后的固体放在干燥器中冷却,再测定出剩余固体的质量,然后根据固体质量变化计算水的质量,从而求算胆矾中的结晶水。
①加热所用到的仪器除了酒精灯、三角架之外还有 。
②如果实验过程中测得的结晶水含量偏高,可能的原因有 (写出一种可能,忽律操作引起的误差)
(1)a (2分)
(2)调节pH,使三价铁离子完全沉淀;CuO(或CuCO3或Cu2(OH)2CO3)(2分)
(3)蒸发浓缩;冷却结晶(2分)
(4①坩埚、坩埚钳、泥三角(2分)
②硫酸铜可能部分分解(2分)
通过并不复杂的实验流程图,考察了灼烧等基本实验设计的仪器、以及除杂试剂的选择、误差分析等基本实验知识。实验基础知识结合化学反应原理的考查是近几年的考试新形式。
(1)试剂A的作用是将二价铁氧化为三价铁,但又不能引入新的杂质,所以选a;(2) Cu(OH)2的作用是调节pH,使三价铁离子完全沉淀, 还可以用CuO(或CuCO3或Cu2(OH)2CO3)代替;(3)从溶液中得到含有结晶水的化合物,一般采用蒸发浓缩、冷却结晶再过滤的方法;(4)I.这是将固体灼烧,所以在坩埚中进行与之配套的仪器要写全。II.实验过程中测得的结晶水含量偏高,可能是硫酸铜部分分解。
