问题
计算题
(6分)(2012•宁夏)碳酸钙是牙膏中一种常用的摩擦剂,可用石灰水作原料来制备,某工厂为了测定一批石灰石中所含碳酸钙的质量分数,称取1000g石灰石中样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,冷却,称量剩余固体的质量为648g.已知反应的化学方程式为:CaCO3 CaO+CO2↑,样品中的杂质不参加反应,据此计算:
CaO+CO2↑,样品中的杂质不参加反应,据此计算:
(1)生成二氧化碳的质量.
(2)石灰石样品中碳酸钙的质量分数.
答案
(1)352g(2)80%
(1)根据质量守恒定律,固体减少的质量即为产生二氧化碳气体的质量,生成二氧化碳的质量为1000g﹣648g=352g。
(2)设参加反应的碳酸钙的质量为x,
CaCO3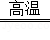 CaO+CO2↑
CaO+CO2↑
100 44
x 352g
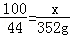 x=800g
x=800g
石灰样品中碳酸钙的质量分数为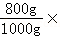 100%=80%.
100%=80%.
答:(1)生成二氧化碳的质量为352g;
(2)石灰样品中碳酸钙的质量分数为80%。
