问题
单项选择题 案例分析题
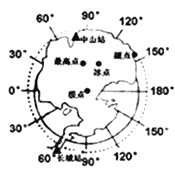
2008年10月20,我国第25次南极科考队从上海港出征。此次科考的任务之一是在南极的最高点(即冰穹A:78°E,80°S)建设我国第三个南极科考站——昆仑站。读图回答下面各题。
近些年来由于环保措施得到有效的执行,南极洲上空的臭氧空洞正在不断缩小,这一现象说明()
A.大气对人类排放的有害气体的自净能力增强
B.人类已经不必关心臭氧空洞等环境问题
C.环境与发展问题得到国际社会的普遍关注
D.50年后,全球变暖等大气环境问题都将得到解决
答案
参考答案:C
解析:
南极洲上空的臭氧空洞主要是人类使用制冷剂,排放氟氯烃。那么近年在不断的减小,主要是因为环境与发展问题越来越得到国际社会的普遍关注。
考点:地球运动的地理意义;中国自然地理。
