维生素C(分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知溶液的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2 C6H6O6+2HI
C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下。取10mL 6mol·L-1CH3COOH,加入100mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.2000g样品,溶解于上述冷却的溶液中,加入1mL淀粉指示剂,立即用浓度为0.05000mol·L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00mLI2溶液。
(1)为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
(2)计算样品中维生素C的质量分数。
(1)煮沸是为了除去溶液中溶液的O2,避免维生素C被O2氧化,冷却是为了减缓滴定过程中维生素C与液面上空气接触时被氧化的速度。
(2)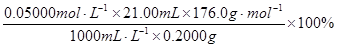 =92.40%
=92.40%
题目分析:维生素C(分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,煮沸是为了除去溶液中溶液的O2,避免维生素C被O2氧化,冷却是为了减缓滴定过程中维生素C与液面上空气接触时被氧化的速度;
解:设样品中维生素C的质量分数为x,则有
C6H8O6 + I2  C6H6O6 + 2HI
C6H6O6 + 2HI
176 1
0.2000x 0.05000mol·L-1×0.021L
X=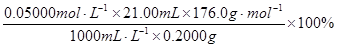 =92.40%
=92.40%
点评:考查了化学计算中的浓度的计算,不是很难,要求学生能熟练运用定量关系进行计算,考查学生的计算能力。
