为探索植物吸水和吸收无机盐的特点和关系,用相同的培养液分别培养水稻和番茄幼苗。培养一段时间后,分别测定培养液中各种养分的百分含量,并与原培养液(各种养分的相对含量为100%)中各种养分百分含量比较,结果如下表所示。
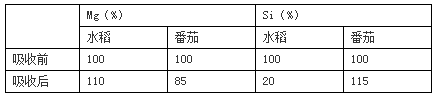
培养水稻的培养液,镁离子的相对浓度比原来升高了,这是由于()。
参考答案:水稻的离子吸收和水分吸收是两个相对独立的过程,溶液中镁离子的浓度比原来升高,说明吸收水的量比吸收镁离子的量相对要多
为探索植物吸水和吸收无机盐的特点和关系,用相同的培养液分别培养水稻和番茄幼苗。培养一段时间后,分别测定培养液中各种养分的百分含量,并与原培养液(各种养分的相对含量为100%)中各种养分百分含量比较,结果如下表所示。

培养水稻的培养液,镁离子的相对浓度比原来升高了,这是由于()。
参考答案:水稻的离子吸收和水分吸收是两个相对独立的过程,溶液中镁离子的浓度比原来升高,说明吸收水的量比吸收镁离子的量相对要多
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥生产等方面有重要应用。请回答下列问题:
(1)砷原子的核外电子排布式为_____________________________________。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为________,该化学键能够形成的原因是______________________________________________________。
(3)NH4+中氮原子的杂化类型为________,NH4+的空间构型为________。
(4)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1 073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是___________________________________________________________________________。
CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是_________________________________________________________________________。
结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时________先液化。
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
请回答下列有关问题:
估计钙元素的电负性的取值范围:________<X<________。经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlCl3中形成的化学键的类型及其理由:__________________________。