问题
选择题
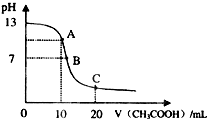
25℃时,在20mL0.1mol•L-1NaOH溶液中逐滴加入0.2mol•L-1醋酸溶液,pH的变化曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
A.在A点:C(Na+)>C(OH-)>C(Ac-)>C(H+)
B.在B点:C(Na+)=C(Ac-)>C(OH-)=C(H+)
C.在C点:C(Ac-)+C(HAc)=2C(Na+)
D.在C点:C(Ac-)>C(Na+)>C(H+)>C(OH-)
答案
A.在A点醋酸和NaOH恰好中和生成NaAc,为强碱弱酸盐,水解呈碱性,但Ac-水解程度较小,应为c(Ac-)>c(OH-),故A错误;
B.B点呈中性,应为C(Na+)=C(Ac-)>C(OH-)=C(H+),故B正确;
C.C点时,n(NaOH)=0.02L×0.1mol/L=0.002mol,n(HAc)=0.02mol/L×0.02L=0.004mol,根据物料守恒可知c(Ac-)+c(HAc)=2c(Na+),故C正确;
D.C点醋酸过量,溶液呈酸性,应存在C(Ac-)>C(Na+)>C(H+)>C(OH-),故D正确.
故选A.
