称取镁和铜的混合物10g于烧杯中,然后取某稀硫酸100g,平均分成4次加入其中,充分反应后实验数据如下表所示:
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
| 生成氢气的总质量/g | 0.15 | x | 0.4 | 0.4 |
上表中从第__________次起,硫酸过量;
求所用稀硫酸的溶质的质量分数。
(1) 0.3 (2) 3 (3) 29.4%
题目分析:向镁和铜的混合物中加入稀硫酸,由于Mg>H>Cu,故镁能反应产生氢气,而铜不能。
(1)根据表格中的数据可知,当第1次加入25g稀硫酸后,生成氢气的质量为0.15g;而第3次加入25g稀硫酸后,生成氢气的质量为0.4g,说明第1次加入的25g稀硫酸完全反应,而镁有剩余(会与继续加入的硫酸反应产生氢气),由此可知,每加入25g稀硫酸后,都能生成氢气0.15g,故当第2次加入25g稀硫酸后,生成氢气的质量为0.15g×2=0.3g。
(2)由于每加入25g稀硫酸后,都能生成氢气0.15g,故当第3次加入25g稀硫酸后,应生成氢气的质量为0.15g×3=0.45g,但实际只有0.4g,说明此时镁已完全反应,即此时硫酸过量。
(3)根据上面的分析可知,前两次的硫酸都是完全反应,故可根据反应产生的氢气质量,计算出25g稀硫酸中硫酸的质量,进而求出硫酸的质量分数。
解:设25g稀硫酸中硫酸的质量为x。
Mg + H2SO4 = MgSO4 + H2↑
98 2
x 0.15g
98:2=x:0.15g
解得x=7.35g
则所用稀硫酸的溶质质量分数=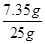 ×100%=29.4%
×100%=29.4%
答:所用稀硫酸的溶质质量分数为29.4%。
点评:此题是关于化学方程式及溶质质量分数的计算题,主要是利用图表及反应方程式来分析和解决化学计算中的有关问题,要求学生有较强的数据分析能力;解题的关键是要明确每次所加稀硫酸与氢气的关系,并能确定第几次加入稀硫酸后镁已完全反应,然后根据相关的化学反应方程式,并依据已知量对未知的应求量进行求解计算即可,注意解题要规范。
