草木灰是农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,化学兴趣小组为测定某草木灰样品中的有效成分,取100草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物的质量为127.8g.
碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4═K2SO4+CO2↑+H2O
(假设草木灰的其他成分不含钾元素,不与酸反应)
请计算回答:
(1)二氧化碳(CO2)分子中,碳,氧元素的原子个数比为
(2)碳酸钾(K2CO3)的相对分子质量为
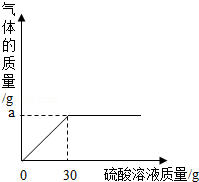
(3)如图表示反应过程放出的气体质量与加入硫酸的关系曲线,请根据质量守恒定律求出图中纵坐标上a点数值:a= g;
(4)草木灰样品中碳酸钾的质量(要求写出计算过程)
(5)通过其他实验,测得该100g草木灰中硫酸钾质量为8.7g,氯化钾质量为2.98g,已知钾肥的有效成分以氯化钾计,则该草木灰样品中氯化钾的质量分数为 %。
(1)1:2;
(2)138;
(3)2.2;
(4)6.9g
(5)2.98.
题目分析:(1)二氧化碳(CO2)分子中,碳,氧元素的原子个数比为1:2;
(2)碳酸钾(K2CO3)的相对分子质量为:39×2+12+16×3=138;
(3)据质量守恒定律可以知道,反应前后减少的质量即为生成的二氧化碳的质量,所以可以求出图中纵坐标上a点数值为:100g+30﹣127.8g=2.2g;
(4)草木灰样品中碳酸钾的质量为x
K2CO3+H2SO4═K2SO4+CO2↑+H2O
138 44
x 2.2g
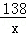 =
=
解得:x=6.9g
答:草木灰样品中碳酸钾的质量为6.9g;
该草木灰样品中氯化钾的质量分数为: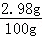 ×100%=2.98%.
×100%=2.98%.
点评:本题主要考查学生运用化学方程式和化学式的相关计算,并考查综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
