问题
填空题
黄铜是Cu和Zn的合金,可用于制造各种仪器零件。为测定黄铜的组成,课外活动小组的同学取黄铜样品10 g放入烧杯中,滴入稀硫酸至不再产生气泡时,测得消耗了稀硫酸30 g,烧杯中剩余固体质量6.1 g。请回答:
(1)测定过程中发生反应的化学方程式为:________________________________。
(2)烧杯中剩余固体的成分为________;黄铜样品中Cu的质量分数为________。
答案
(1)Zn+H2SO4===ZnSO4+H2↑ (2)Cu 61%
题目分析::(1)黄铜中的铜不能和稀硫酸反应,发生反应的为锌和稀硫酸,其中锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(2)黄铜中的铜不能和稀硫酸反应,而加入的稀硫酸又是足量的,所以可以知道剩余的固体为铜,其质量分数为: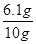 ×100%=61%;
×100%=61%;
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识按照题目要求进行认真地选择或解答即可.
