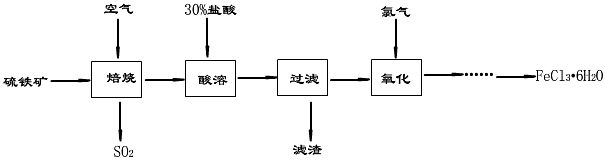
潍坊市继续实施农村集中供水工程,集中供水覆盖人口已达90%以上。自来水厂常用氯气消毒杀菌,用明矾、氯化铁等絮凝剂净化水。以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
回答下列问题:
(1)流程中需用30%的盐酸“酸溶”焙烧后的残渣(主要成分氯化铁),写出反应的方程式_________________________________________________________。
(2)二氧化硫能形成酸雨,危害环境。常用下列方法除去:
方法1. 将含二氧化硫的废气通入氨水中吸收二氧化硫。氨水的pH__________7(填写“大于”、“小于”或“等于”)。
方法2.将含二氧化硫的废气通入石灰石的悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫,写出反应的方程式______________________________________________________。
(3)自来水常用电解饱和食盐水制备消毒剂Cl2,反应的方程式为
2NaCl+2H2O 2NaOH+ Cl2↑+ H2↑。现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?同时生成烧碱多少吨?
2NaOH+ Cl2↑+ H2↑。现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?同时生成烧碱多少吨?
(1)Fe2O3+6HCl=FeCl3+3H2O(2分)
(2)大于(1分) 2SO2+2CaCO3+O2=2CaSO4+2CO2(2分)
(3)80t
(1)氧化铁和盐酸反应的化学方程式为:Fe2O3+6HCl=FeCl3+3H2O;(2)含二氧化硫的废气通入石灰石悬浊液中的化学方程式根据化学方程式的书写步骤写出即可,注意有氧气参与反应;(3)依据化学方程式,设出未知量,代入已知量计算即可。
(3)[解]设:电解的氯化钠的质量为x,生成烧碱的质量为y。
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
2×58.5 2×40 71
x y 71t
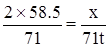 x=117t (2分)
x=117t (2分)
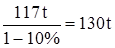 (1分)
(1分)
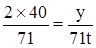 y=80t (2分)
y=80t (2分)
答:需要含杂质10%的粗盐130t,生成烧碱的质量为80t。
