小亮同学对在空气中放置一段时间的“铜树”(铝丝浸泡在硫酸铜溶液制成如右图)的的成分时行分析,取出64.1克固体样品,用10%的盐酸充分溶解,溶液呈无色,产生的气体和剩余固体随消耗10%的盐酸质量变化关系曲线如下图:
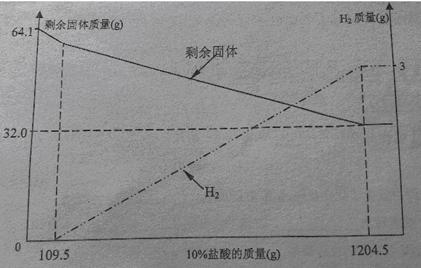
结合图中数据分析:
(1)读图可知,Cu元素的质量_____g,64.1g“铜树”有Cu、Al、_____(填化学式)
(2)请结合化学方程式计算该“铜树”中Al元素的质量分数?
(3)只知道“铜树”质量m1和消耗10%的盐酸总质量(m2),也能求出“铜树”中铝元素质量分数,其表达式为_______________(用m1和m2表示,可不化简)
(1)32.0 Al2O3 (2)64.3% (3)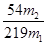 ×100%
×100%
(1)铜不与盐酸反应,Al能与盐酸反应,硫酸铝溶于水,故剩余固体的质量为铜的质量;Al与CuSO4溶液反应,生成Cu和Al2(SO4)3;
(2)设固体样品中Al的质量为x。
2Al + 6HCl = 2AlCl3 + 3H2↑
54 6
x 3g
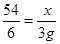
x=27g
Al2O3与稀盐酸反应时,消耗盐酸的质量为109.5g×10%=10.95g
设Al2O3的质量为y,
Al2O3 + 6HCl = 2AlCl3 + 3H2O↑
219
y 10.95
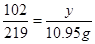
y=5.1g
Al2O3中Al的质量为5.1g×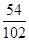 ×100%=2.7g
×100%=2.7g
样品中Al的质量为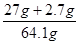 ×100%=46.3%
×100%=46.3%
答:该“铜树”中Al元素的质量分数为46.3%。
