问题
计算题
为测定某碳酸钠溶液的溶质质量分数,小虎取100g该溶液,向其中滴加11.1%的氯化钙溶液直至不再产生沉淀,共用去氯化钙溶液100g,反应的化学方程式为:Na2CO3+CaCl2=2NaCl+CaCO3↓.求:
(1)碳酸钠溶液的溶质质量分数;
(2)反应后所得溶液的溶质质量分数(结果保留至0.1%).
答案
(1)10.6% (2)6.2%
题目分析:(1)设碳酸钠溶液的溶质质量为x、与氯化钙反应生成的氯化钠的质量为y,碳酸钙的质量为z
氯化钙的质量为:100g×11.1%=11.1g
Na2CO3+CaCl2=2NaCl+CaCO3↓
106 111 117 100
x 11.1g y z
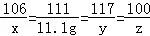
解得:x=10.6g y=11.7g z=10g
碳酸钠溶液的溶质质量分数为: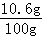 ×100%=10.6%
×100%=10.6%
(2)反应后所得溶液的溶质质量分数为: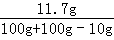 ×100%=6.2%
×100%=6.2%
答:(1)碳酸钠溶液的溶质质量分数为10.6%;
(2)反应后所得溶液的溶质质量分数为6.2%.
点评:本题主要考查学生运用化学方程式进行计算的能力.学生须认真分析题意,找出各物质间的关系,正确写出方程式,并能根据质量分数公式计算,才能正确解答.
