问题
计算题
2012年4月15日,央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊.在熬制过程中添加重铬酸钾(K2Cr2O7),导致生产的药用胶囊重金属铬超标.根据化学式计算:
(1)该物质由 种元素组成.
(2)钾、铬、氧三种元素的质量比 (要求填最简整比).
(3)铬元素的质量分数 (结果保留到0.1%).
(4)29.4g该物质中含有钾元素的质量为 g.
答案
(1)三;(2)39:52:56;(3)35.4%;(4)7.8.
题目分析:(1)重铬酸钾(K2Cr2O7)由钾、铬、氧三种元素组成;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比为:(39×2):(52×2):(16×7)=39:52:56;
(3)根据物质中某元素的质量分数= ×100%,可得重铬酸钾中铬元素的质量分数为:
×100%,可得重铬酸钾中铬元素的质量分数为: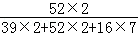 ×100%=35.4%;
×100%=35.4%;
(4)29.4g重铬酸钾中含有钾元素的质量为29.4g×(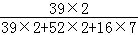 ×100%)=7.8g.
×100%)=7.8g.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
