葡萄糖是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程。
| 部分性质 | 生理作用 | |
| 葡萄糖 化学式: C6H12O6 | 白色结晶或颗粒状粉末,味甜;易溶于水;具有还原性,葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀 | 葡萄糖为机体所需能量的主要来源,能促进肝脏的解毒功能,对肝脏有保护作用 |
请参与下列问题的讨论:
(1)葡萄糖中碳、氢、氧三种元素的质量比为 。
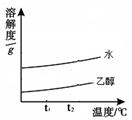
(2)某兴趣小组的同学对葡萄糖的溶解性进行实验探究,其实验结果如图所示。实验说明了葡萄糖的溶解性除跟温度有关外,还与 有关。现用10g纯净的葡萄糖,则理论上可配制5%的葡萄糖溶液 g。
(3)该兴趣小组同学对某样品中葡萄糖的含量进行测定,反应原理为:C6H12O6+2Cu(OH)2 C6H12O7+Cu2O↓+2H2O
C6H12O7+Cu2O↓+2H2O
实验步骤如下:a.取样品20g于烧杯中,用蒸馏水溶解到50 mL;
b.加入新制的新制氢氧化铜悬浊液;
c.加热;
d.实验完毕后称得生成砖红色沉淀的质量为14.4g。计算该样品中葡萄糖的质量分数为多少? (请将计算过程写在答题纸上)
(1)6:1:8。(2)溶剂、200g。(3)90%
题目分析:(1)元素的质量比是元素原子量和的比,则葡萄糖中碳、氢、氧三种元素的质量比为:(12×6):12:(16×6)=6:1:8;(2)根据溶解度曲线可知葡萄糖的溶解性除跟温度有关外,还与溶剂的种类(性质)有关;用10g纯净的葡萄糖,则理论上可配制5%的葡萄糖溶液的质量为:10g/5%=200g
(3)根据在化学反应中各物质质量成比例,所以可以根据沉淀Cu2O的质量求出C6H12O6的质量,即可计算该样品中葡萄糖的质量分数。
设:生成14.4g砖红色沉淀,需要C6H12O6的质量为X
C6H12O6+2Cu(OH)2 C6H12O7+Cu2O↓+2H2O
C6H12O7+Cu2O↓+2H2O
180 144
X 14.4g
180/X=144/14.4g 解得:X=18g
所以该样品中葡萄糖的质量分数为:18g/20g=90%
