(7分)元素周期律和周期表是研究化学的重要工具。下表是元素周期表的部分信息。
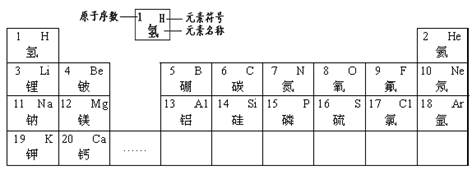
请认真分析表中信息,回答下列问题。
(1)从原子结构看, Na和Mg同属于第三周期的原因是 ,F和Cl属于同一个族的原因是 。
(2)从元素种类看,每一周期从左到右由 元素过渡到 元素,并以稀有气体元素结束。
(3)由8和13号两种元素组成的化合物是 (写化学式)。
(4)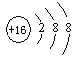 如左图的结构示意图表示的是 (写粒子符号)。
如左图的结构示意图表示的是 (写粒子符号)。
(5)根据下表中相关信息,判断出的元素名称不一定合理的是 (选填序号)。
(1)原子的电子层数为3(若写“原子的电子层数相同”给0.5分)
原子的最外层电子数都为7(若写“原子的最外层电子数相同”亦可)
(2)金属 非金属 (3)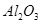
(4)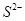 (5)B
(5)B
本题考查的是元素周期表的特点及其应用。
(1)从原子结构看,同一周期的原子核外电子层数相同,同一族的原子最外层电子数相同,故Na和Mg同属于第三周期的原因是原子的电子层数为3,F和Cl属于同一个族的原因是原子的最外层电子数都为7。
(2)根据元素周期律:每一周期从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束。
(3)8和13号两种元素分别是氧和铝,故它们组成的化合物是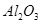 。
。
(4)根据原子结构示意图的特点:非金属元素的最外层电子数一般多于4,易得到电子,形成阴离子;根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字;离子符号表示为S2-。
(5)最外层电子数是8的粒子,不一定原子,可能是离子,故B错误。
