问题
选择题
下列比较中,正确的是( )
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B.0.2 mol·L-1NH4Cl和0.1 mol·L-1NaOH溶液等体积混合后:
c(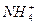 )>c(Cl-)>c(Na+)>c(OH-)>c(H+)
)>c(Cl-)>c(Na+)>c(OH-)>c(H+)
C.物质的量浓度相等的H2S和NaHS混合溶液中:
c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D.同浓度的下列溶液中,①(NH4)2SO4、②NH4Cl、③CH3COONH4、④NH3·H2O;c(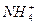 )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
答案
答案:D
由“HF比HCN易电离”可知CN-的水解程度大于F-的水解程度,两者水解都使溶液显碱性,所以同温度同物质的量浓度时,则NaF溶液的pH比NaCN溶液小,A项错误;B项反应后的溶液相当于浓度相等的NaCl、NH3·H2O、NH4Cl三种溶液混合,所以c(Cl-)>c(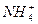 );由电荷守恒可知,C项应为c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)。
);由电荷守恒可知,C项应为c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)。
