(7分)中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。
(1)下图表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线。请从曲线图中获取信息,回答下列问题:
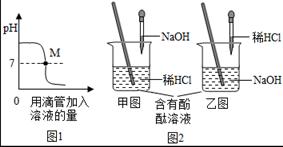
①图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化。进行该反应的实验操作是按照图2中的 (填甲或乙)图所示进行的。
②曲线上M点表示 。
③向烧杯中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为 色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为 (结果精确到0.1%)。
(2)为证明中和反应是放热反应,某小组进行了如图所
示的实验操作:
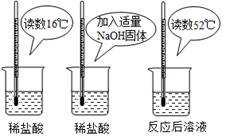
根据上图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应。乙同学认为:甲同学得出
这个结论的依据不科学,理由是 。
(3)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、
D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,
再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
| 烧杯编号 | A | B | C | D | E |
| 盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
| 反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
交流反思:反应后,烧杯内溶液pH最小的是 (填烧杯编号)。
(1)①乙 ②盐酸和氢氧化钠恰好完全反应 ③无 2.9%
(2)氢氧化钠固体溶于水也会放出大量的热
(3)盐酸的浓度越大,放出的热量越多 E
题目分析:①从图1图象可知,该反应开始时是碱性,随着另一种物质的加入溶液逐渐变为中性至酸性;所以反应应为向氢氧化钠溶液中加盐酸。即进行该反应的实验操作是按照图2中的乙图所示进行的。
②曲线上M点对应的PH值为7,表示盐酸和氢氧化钠恰好完全反应。
③开始的氢氧化钠溶液呈碱性,可使无色酚酞变红。根据化学方程式计算可知:当加入的稀盐酸20 g时,二者恰好完全反应,溶液呈中性显无色。
根据题意可知,已知量为:氢氧化钠的质量;未知量为反应后溶液中溶质(为氢氧化钠与盐酸反应生成的氯化钠)质量分数。
解题思路:可根据二者在反应中的质量关系,先求解出生成氯化钠的质量。根据反应可知,所得溶液的质量为所用的氢氧化钠溶液的质量和稀盐酸溶液的质量的和。可进一步求出溶液中溶质的质量分数。具体解题过程为:
解:设生成氯化钠的质量为x
NaOH + HCl====NaCl+H2O
40 58.5
20g×4.00% x
40:58.5=(20g×4.00%):x
x=1.17g
所得溶液中溶质的质量分数为: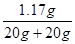 ×100%≈2.9%
×100%≈2.9%
(2)氢氧化钠固体溶解于水时,也能放出热量,所以不能确认是氢氧化钠与稀盐酸反应放热。
(3)根据表中数据可知:当盐酸的浓度越大的时,反应后溶液的温度越高;所以可说明盐酸的浓度越大,放出的热量越多。
交流反思:根据氢氧化钠与盐酸反应的质量关系可知:当盐酸的质量分数为20%时,二者恰好完全反应,所以所得的D溶液为中性;ABC三溶液为碱性;E为酸;所以反应后,烧杯内溶液pH最小的是E。
