(14分)化学是研究物质的组成、结构、性质及变化规律的科学。
(1)①铜、②干冰、③氯化钠三种物质中,由离子构成的是 (填写序号,下同),可用于人工降雨的是 。
(2)食醋中含有醋酸(CH3COOH),醋酸由 种元素组成,其分子中氢、氧原子个数比为 。
(3)气体A和气体B接触可发生反应,生成固体C和液体D,其微观过程如下所示。
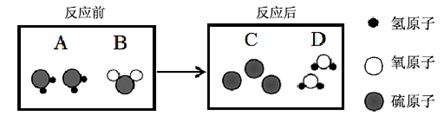

图1 图2
① 该反应过程中,属于氧化物的是 (填名称)。
② 将等体积的两只集气瓶中分别盛满A、B,如图2所示进行实验。已知相同条件下,气体的体积比等于分子个数比, 则充分反应后,剩余的气体是 (填化学式)。
(4)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
① 用pH试纸检测废水呈碱性的方法是 。
② 若某造纸厂废水中含NaOH的质量分数为l.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可以处理的废水质量是多少?(写出计算过程)
(1)③ ② (2)3 2:1 (3)① 二氧化硫、水(多写不给分,少写1个给1分) ② SO2(4)①在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取废水滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出废水pH。②100t
题目分析:(1)①铜、②干冰、③氯化钠三种物质中,由离子构成的是③氯化钠,可用于人工降雨的是② 干冰;(2)食醋中含有醋酸(CH3COOH),醋酸由三种元素组成,其分子中氢、氧原子个数比为2:1;(3)① 该反应过程中,属于氧化物的是有了两种元素组成且一种元素是氧元素的化合物,故二氧化硫、水;② 将等体积的两只集气瓶中分别盛满A、B,如图2所示进行实验。已知相同条件下,气体的体积比等于分子个数比, 则充分反应后,根据反应中的分子个数比,可知剩余的气体是二氧化硫SO2;(4)① 用pH试纸检测废水呈碱性的方法是在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取废水滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出废水pH;
②解:设可以处理的废水的质量为x 0.5分
2NaOH + H2SO4 = Na2SO4 + 2H2O 1分
80 98
1.6%x 9.8t×20% 1分
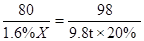 1分
1分
x=100t 1分
答:可以处理的废水的质量为100t 0.5分
