(9分)某溶液中可能含有碳酸钠、氯化钾、硫酸钠、硫酸中的一种或几种,为测定其组成,进行如下实验:
取样20g,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示.
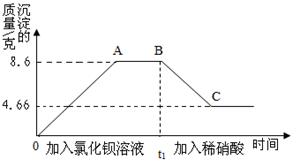
(1)实验中,AB之间图象所对应的溶液中的溶质一定有 .
(2)BC段沉淀减少的原因是 (用化学方程式表示).
(3)由上述实验可知,原溶液中一定含有 ,可能有 .
(4)求原溶液中硫酸钠的质量分数。
(1)NaCl和BaCl2 (2) BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O
(3)Na2CO3和Na2SO4 KCl (4) 14.2%
题目分析:(1)从图中BC段,加入稀硝酸后,沉淀质量减少但并没有减少为0,说明沉淀中既有BaCO3又有BaSO4,说明加入氯化钡溶液,OA段发生了2个反应:Na2SO4+BaCl2==BaSO4↓+2NaCl和Na2CO3+BaCl2==BaCO3↓+2NaCl,AB段表示氯化钡过量,所以AB之间图象所对应的溶液中的溶质一定有NaCl和BaCl2
(2)BC段沉淀减少的原因是:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O
(3)根据上述实验分析可知,原溶液中一定含有Na2CO3和Na2SO4,由于硫酸与Na2CO3不能共存,所以一定不含硫酸,可能有KCl
(4)从图象分析可知,加入稀硝酸后,最终仍有4.66g沉淀未溶解,即为BaSO4的质量,所以可根据方程式:Na2SO4+BaCl2==BaSO4↓+2NaCl中Na2SO4和BaSO4的质量关系,即可求出Na2SO4的质量,进而可计算原溶液中硫酸钠的质量分数
解: 设原溶液中硫酸钠的质量为X。
Na2SO4+BaCl2 ==BaSO4↓+2NaCl
142 233
X 4.66g
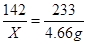 X=2.84g
X=2.84g
Na2SO4%=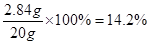 32-、SO42-的检验,根据方程式计算
32-、SO42-的检验,根据方程式计算
