实验室配制有0.1mol/L的Na2CO3溶液,根据电离平衡和水解知识,回答下列有关问题:
⑴写出H2CO3的电离方程式为 ;
⑵Na2CO3溶液显碱性,原因是(用离子方程式表示)
;(2分)
⑶在该溶液中,c(Na+)、c(CO32-) 、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;(2分)
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;(2分)
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。(2分)
⑴H2CO3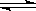 H++HCO3-(以第一步为主)HCO3-
H++HCO3-(以第一步为主)HCO3-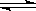 H++CO32-;
H++CO32-;
⑵CO32-+H2O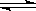 OH-+HCO3-(以第一步为主)(2分) HCO3-+H2O
OH-+HCO3-(以第一步为主)(2分) HCO3-+H2O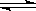 H2CO3+OH-;
H2CO3+OH-;
⑶c(Na+)>c(CO32-)>c(OH-) >c(HCO3-)>c(H+);
⑷c(HCO3-)+c(OH-)+2c(CO32-);(2分)
⑸2[c(HCO3-)+c(H2CO3)+c(CO32-) ](2分)
